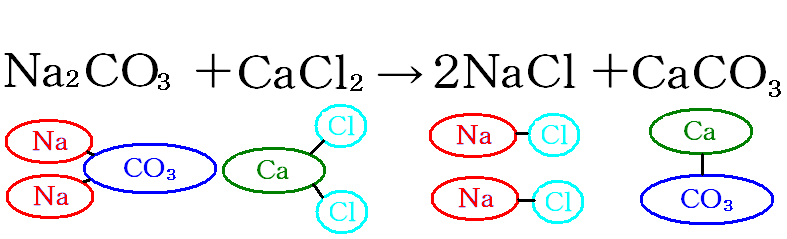化学の実験の中でも、沈澱のできる実験というのは目を見張る物があります。
しかし、難しい薬品などを使わなければできない物も多く、ほとんどが家で出来ません。
そこで今回、tritonのブログにも書いた、炭酸ナトリウムと塩化カルシウムによる沈澱の実験をします。
では下に、列挙して見ます。
使用する薬品類
- 炭酸ナトリウム(後ほど説明)
- 塩化カルシウム(融雪剤に使われる物。後ほど説明)
- 水(今回は薬品としてつかいます)
使用する道具類
- ゼリーなどの空きカップ・・・2つ(今回は分かりやすいように2つのカップをそれぞれ違うものにしました)
- スプーン(プラのスプーンで十分です。)
- スポイド(必須ではありませんが、あると便利です)

今回は結構少なめに済みました。
ではまず、炭酸ナトリウムから説明していきます。
炭酸ナトリウムは、炭酸水素ナトリウム(別名:重曹)を熱分解して得る事ができます。
お家に炭酸ナトリウムが無い場合は、こちらの方法で重曹から作ってください。
続いて塩化カルシウムですが、これは主に、道路の融雪剤として使われています。
冬になると大袋が路肩においてあると思うので、それをいくらか拝借してくるといいでしょう(コラ)
では、実験を始めます。
まず、2種類の水溶液を作ります。
最初に塩化カルシウムから作っていきましょう。塩化カルシウムをスプーンに1杯とって、半分ぐらいにまで水を張った空きカップに入れます。

ある程度かき混ぜたら、そのスプーンを一度洗って、炭酸ナトリウムの水溶液を作ります。
塩化カルシウム同様、炭酸ナトリウムを1杯とって、なるべく飽和水溶液になるように水に溶かします。
そして、この炭酸ナトリウム水溶液を、A液とします。
さて、2種類の水溶液が出来ました。では早速沈澱を作りましょう!
A液を、塩化カルシウム水溶液に注いでみてください。見る見るうちに、白い沈澱が生じているのが分かるはずです!(一応スポイドを使いました。)

そしてかき混ぜると、完全に反応します。

さて、この沈澱は何かといいますと、(ブログを見た方は知ってるかも)チョークの主成分である炭酸カルシウムなんです。そして、液体の方は塩化ナトリウムの水溶液になっています。では、反応を下に示します。
Na2CO3 + CaCl2 → 2NaCl + CaCO3
ここで、あることに気づいたわけです。NaとCaがそっくりそのまま入れ替わってる!!!
分かりやすいように下に図解します。
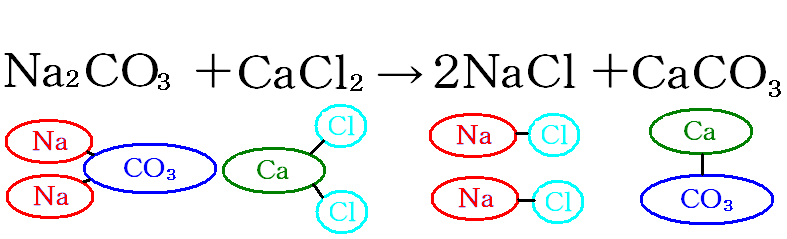
分かっていただけたでしょうか?確かに入れ替わってますね。
つまり、この2種類の物質は交換をしているといえるわけです。
偶然から生まれたこの反応ですが、これから何かに使えたらイイナァと思っています(たぶん使えない)。
この実験は危険な薬品を使う事も無く、火も使わないので、安心して取り組む事ができます。
また、実験器具など難しい特別な物を使う必要も無いので手軽に出来ます♪
このように、新たな発見は偶然から導かれる事も多いわけです。だれでも、大発見をする要因は持っています。
さて、ではこの辺で第3回になる実験を終わります。
これらについての疑問・質問・訂正箇所などあれば、「雑談の間」の北海道エリアにカキコお願いします。
大歓迎ですので、気軽にどうぞ!
雑談の間へ
気まぐれの間に戻る
トップへ戻る